Beim Thema BCAA hat sich in den letzten Monaten so einiges getan. Einst eines der beliebtesten Supplements für Sportlerinnen und Sportler überhaupt, berichten heute nahezu alle Anbieter von rückläufigen Verkäufen. Die Beliebtheit von BCAA befindet sich im freien Fall da man offensichtlich erst jetzt bemerkt hat, wie dünn die Datenlage zu echten Vorteilen einer Verabreichung ausfällt. Die Szene lernt und setzt sich nun über das geschickte Marketing angeblich antikataboler, muskelaufbauender Aminosäuren hinweg.
Weit vor der großen Trendwende von BCAA zu EAA habe ich bereits im September 2016 auf das enorme Potenzial von EAA anstelle von BCAA hingewiesen und in diesem Zusammenhang HBN EAA CODE vorgestellt (1). Zum Zeitpunkt der Erstellung dieses Beitrags sind Hersteller nun bemüht allesamt neben BCAA zwingend auch eine EAA-Matrix auf den Markt zu werfen um den Zug nicht zu verpassen. Noch einen Schritt weiter gibt es eine weitere Bewegung die sich weder für BCAA noch für EAA ausspricht und behauptet, beide hätten verglichen mit hochwertigem Protein wie beispielsweise Wheyprotein keinerlei Vorteile. Meinungen wie diese finden ihre Intention aller Wahrscheinlichkeit nach im Bestreben Whey-Hydrolisat oder eine andere Whey-Matrix aus deren Shops oder Produktportfolios an den Mann zu bringen, anders kann ich mir derartige Aussagen nicht erklären.
Mein neuer 2-Teiler ist ein Sammelsurium unterschiedlichster Meinungen und Studien die in den vergangenen Monaten zum Thema BCAA veröffentlicht wurden. Wir sind der Wahrheit auf der Spur! Los geht es heute mit dem Einsatz von BCAA für Muskelaufbau, für eine beschleunigte Regeneration, gegen Muskelkater und vorzeitige Ermüdung unter Belastung.
Viel Spaß

THEMA 1 – BCAA FÜR MUSKEAUFBAU
The Muscle PhD – „Which BCAA is most potent?”
Als unbestritten gilt, dass BCAA in der Lage sind die Proteinsynthese anzuregen. Beigefügte Darstellung relativiert den Einfluss
- einerseits dahingehend, dass nur Leucin ein wirklich nennenswerter Effekt zugesprochen werden kann
- andererseits dahingehend, dass bei Garlick (2) vollständiges Protein denselben Effekt auf die Proteinsynthese ausübte wie dieser bei BCAA messbar war
- letztlich in dem klar gestellt wird das BCAA Proteinsynthese nur signalisieren, Proteinaufbau mangels der anderen essentiellen Aminosäuren aber niemals selbst bewerkstelligen könne
Halten wir fest:
Alleine Leucin verdanken BCAA den starken Signaleffekt auf die Proteinsynthese. Dabei ist es entscheidend zu wissen das Proteinaufbau mit BCAA andres als mit EAA oder vollständigem Protein nicht möglich ist
„Krafttraining ist schon genug Stimulus“
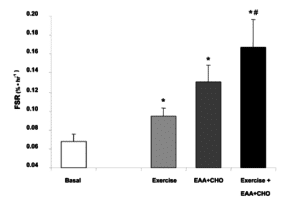
Immer wieder hört und liest man Aussagen nach denen Training alleine schon für eine maximierte Stimulierung der Proteinsynthese sorgen würden. FALSCH, zeigt beigefügte Darstellung. Tatsächlich lässt sich die Proteinsynthese mit der Einnahme von EAA (20g) und Kohlenhydraten (30g) stärker anregen als dies mit Krafttraining ohne gleichzeitige Verabreichung von Nährstoffen im Anschluss der Falls ist. Kombiniert man beides führt dies nochmal zu einem signifikanten Anstieg der Proteinsynthese-Reaktion sofern (wie hier) die Verabreichung der Nährstoffe binnen einer Stunde nach dem Training stattfindet (39).
entnommen aus (39)
Halten wir fest
Es erscheint durchaus sinnvoll die Proteinsynthese neben Krafttraining auch mit der Zufuhr von Aminosäuren zu stimulieren
BCAAs and Muscle Growth: Complete Sense or Nonsense?
Weiter geht es mit einem Beitrag von Adam Virgile in seinem BLOG ShakeBot. Er trifft gleich zu Beginn die Aussage der Notwendigkeit von ausschließlich EAA zur Förderung von Proteinaufbau (23-26). Trotz seines Einflusses auf die Proteinsynthese sei die zusätzliche Einnahme von Leucin als eine der BCAA nur in Verbindung mit suboptimaler Proteinversorgung sinnvoll (27). Wenn ausreichend EAA anwesend sind geht von einer zusätzlichen Leucin-Verabreichung kein zusätzlicher Nutzen aus, auch nicht in Verbindung mit Training (28). Diese Aussage bestätigt auch die Arbeit von Aguiar et al (66) an jungen trainierten Probanden.
Eine dauerhafte (16 Stunden) Verabreichung von BCAA via Infusion sorgt sogar für eine Abnahme der Muskelproteinsynthese bei gleichbleibendem Muskelproteinabbau (29,30). Begründen lässt sich dies über eine entstehende Unverhältnismäßigkeit im Aminosäure-Pool. In diesem Zusammenhang stellt er die Bedeutung der sog. limitierenden Aminosäure als wichtige Größe für den Proteinstoffwechsel heraus. Fehlt es auch nur an einer der EAA spielt es keine Rolle wie viele wir von den anderen Aminosäuren verfügbar haben oder einnehmen. Die limitierende Aminosäure ist es die der Muskelproteinbildung den Riegel vor schiebt wie beigefügte Darstellung zeigt.
Studien wie von Jackman et al (31) weisen mit der Einnahme von 5,6g BCAA verglichen mit Placebo eine höhere Stimulierung der Proteinsynthese um 22% nach. Ein solcher Anstieg ist erstens bei weitem nicht das was tatsächlich möglich wäre, zweitens bedeutet die Anhebung anaboler Signalkaskaden nicht automatisch auch eine vermehrte Proteinsynthese. Gemessen wurde der echte Proteinaufbau in genannter Studie nicht, aus anderen Untersuchungen wie der von Blomstrand (32) geht jedoch hervor, dass Muskelproteinsynthese nur dann stattfindet, wenn alle EAA in ausreichender Menge vorhanden sind. Tatsächlich schafft es eine kleine Menge EAA (3g) auch ohne jegliche anabole Signalkaskade die Muskelproteinsynthese zu stimulieren (33).
Anmerkung
Passend dazu der Passus aus einer Studie von Morton et al (38) die sich mit nutritiven Strategien für vermehrte Muskelhypertrophie auseinandersetzt:
„Despite the popularity of BCAA supplements we find shockingly little evidence for their efficacy in promoting MPS or lean mass gains and would advise the use of intact proteins as opposed to a purified combination of BCAA that appear to antagonize each other in terms of transport both into circulation and likely into the muscle”
Branched-Chain Amino Acid Ingestion Stimulates Muscle Myofibrillar Protein Synthesis following Resistance Exercise in Humans
Die oben bereits zitierte Studie (31) liefert weitere wichtige Informationen für die Eingrenzung der Effekte von BCAA. Mit 5,6g BCAA (die in 20g Wheyprotein enthaltene Menge) trat nach Krafttraining eine 22% stärkere Stimulierung der Muskelproteinsynthese ein als dies mit einem Kohlenhydrat-Placebo nachweisbar war. Das Ergebnis fiel damit jedoch um 50% geringer aus als es mit besagten 20g Wheyprotein gemessen wurde und das trotz derselben Netto-BCAA-Menge. Die Forscher begründen die Unterschiede über die begrenzte Verfügbarkeit der anderen EAA. Die vollständige Verfügbarkeit aller essentiellen Aminosäuren gelte als limitierender Faktor für eine maximierte Muskelproteinsynthese insbesondere nach körperlicher Belastung (35,36).
Fazit
Der alleinige Effekt von BCAA geht nicht über eine Stimulierung der Proteinsynthese hinaus. Dies vermögen BCAA zudem weniger effektiv als EAA oder ein hochwertiges vollständiges Protein. Proteinsynthese zu signalisieren bedeutet nicht gleich Protein aufzubauen. Ob es dazu kommt entscheidet sich nicht über die Verfügbarkeit von BCAA, sondern von allen zum Proteinaufbau benötigten essentiellen Aminosäuren (EAA). Werden BCAA additiv zu einer ausreichenden EAA-Versorgung verabreicht sind Effekte unwahrscheinlich. Werden BCAA additiv zu unzureichender Aminosäureversorgung verabreicht können sie von Vorteil sein sofern eben Leucin, Isoleucin oder Valin derzeit die limitierenden Aminosäuren darstellen. Einzig einen Einfluss auf trainings-induzierte Muskelschäden sieht Adam Virgile als möglichen Effekt von BCAA sofern diese in richtiger Art und Weise wie bei Foure et al (34) verabreicht werden. Hierzu kommen wir gleich.

THEMA 2 – BCAA UND REGENERATION
“BCAA Bashing: Have The Big Three Of Aminos Been Debunked As Muscle-Builders?”
Chris Lokwood äußerte sich auf Bodybuilding.com ebenfalls zu BCAA vs. EAA. Er bestätigt die tragendere Rolle von EAA verglichen mit BCAA für die Reaktion des Proteinstoffwechsels auf Krafttraining im nüchternen Zustand für Muskelaufbau. Weiter fügt er hinzu, dass weder BCAA noch EAA hierfür als Ergänzung nötig wären wenn die Proteinbilanz via natürlichen Lebensmittel im Rahmen des individuellen Bedarfs gedeckt werden kann (hört hört…). Aus einer Korrespondenz mit Dr. Juha Hulmi gehen seiner Meinung nach dennoch folgende mögliche Einsatzmöglichkeiten von BCAA hervor:
- eiweißarme Ernährung
- Niedrige Leucin-Verfügbarkeit z.B. bei Veganern
- Ergänzung zu einer eiweißarmen Mahlzeit vor dem Schlafen gehen
- Vor einem Wettkampf
Weiter heißt es, dass BCAA durchaus das Potenzial aufweisen Muskelanabolismus zu unterstützen, allerdings nicht derart effektiv wie dies mit EAA oder vollständigem Protein zu erwarten sei (5,6). In Bezug auf eine Übersichtsarbeit aus 2015 (7) nennt der Autor reduziertes Schmerzempfinden, verringerte wahrgenommene Anstrengung, später eintretende Ermüdung, weniger Muskelschäden, eine verbesserte Regeneration des Muskelapparats und auch des Immunsystems als potentielle Effekte von BCAA in Kontext zum Training von Ausdauersportlern. Problematisch gestaltet sich, dass es hierfür offensichtlich keine genaue Empfehlung für die effektivste Einnahmemenge oder den optimalen Einnahmezeitpunkt gibt. Lediglich beim Verhältnis der BCAA zueinander scheint 2/3:1:1 Vorteile zu bergen. 0,2g BCAA pro Tag über mindestens 10 Tage vor dem Training müsse man einer weiteren Übersichtsarbeit (8) mit einer nur kleinen Anzahl involvierter Studien zur Folge zu sich nehmen, um damit das Ausmaß von Muskelschäden zu verringern.
Meine Anmerkungen zu den genannten Einsatzmöglichkeiten von BCAA
Niedrige Leucin-Verfügbarkeit z.B. bei Veganern
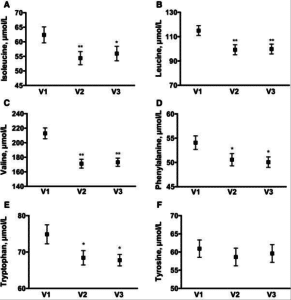
Tatsächlich geht aus Studien (3,4) hervor, dass pflanzlich basierte Kost insgesamt weniger Leucin liefert und zu niedrigen Muskelproteinsynthese-Raten beiträgt:
entnommen aus (3)
entnommen aus (4)
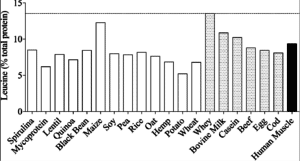
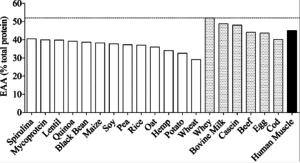
ABER – Das Problem der veganen Ernährung ist nicht alleine Leucin sondern der gesamte EAA-Gehalt wie beigefügte Darstellung zeigt. Aus diesem Grund stellt die Verwendung pflanzlich basierter EAA Produkte wie HBN EAA CODE eine willkommene Ergänzung für vegane Diäten dar die insgesamt sinnvoller erscheint als die alleinige Zufuhr von BCAA.
entnommen aus (4)
Eiweißarme Ernährung
Ergänzung zu einer eiweißarmen Mahlzeit vor dem Schlafen gehen
Die Einnahme von BCAA ergänzend zu einer eiweißarmen Mahlzeit oder generell bei eiweißarmer Ernährung gestaltet sich unschlüssig, da wenig Gesamtprotein bedeutet, dass es nicht nur an BCAA sondern an allen EAA mangelt. Folglich wäre auch hier die Verabreichung einer vollständigen EAA-Matrix sinnvoller als lediglich BCAA zuzuführen. Interessant sind hier die unterschiedlichen Möglichkeiten EAA einmal ergänzend zu einem geringen Eiweißanteil aus der Nahrung einer Mahlzeit zu verwenden, oder eben den gesamten Proteingehalt der Mahlzeit durch EAA zu ersetzen, was bis zu einer Aufnahmemenge von 10g Gesamt-EAA durchaus sinnvoll erscheint (67).
Weniger Müdigkeit – Weniger Muskelkater – Schnellere Regeneration
Eine Reihe von Studien zeigt, dass sich späteres Eintreten von Müdigkeit im Rahmen einer Belastung ausgelöst über den Serotoninmindernden Effekt von BCAA im Gehirn (68,69) nicht zwangsläufig auch auf die tatsächliche körperliche Leistungsfähigkeit auswirkt (9-13). Weiter scheint der Effekt bei untrainierten Personen wirkungsvoller zu sein als bei trainierten Personen (14). All das lässt auf eine hohe Individualität echter Effekt von BCAA in Hinblick auf verminderte Ermüdung und verlängerte Leistungsbereitschaft schließen.
Selbiges lässt sich auch bei der Reduzierung von Muskelkater berichten. Aus einzelnen Studien geht eine BCAA-induzierte Reduzierung von CK und LDH hervor (15,22). Es bestehen Hinweise auf eine deutliche Reduzierung subjektiv wahrgenommener Schmerzen (16-18,22) und sogar auf Leistungsverbesserungen in der auf eine ermüdende Belastung folgenden Trainingseinheit (19,20,22). Was hier nach einem echten Vorteil für BCAA aussieht wurde größtenteils Placebo kontrolliert untersucht, also nach dem Motto: „BCAA sind effektiver als gar nichts zu nehmen“. Es zeigt sich zudem selbst hier eine gewisse Individualität zu erwartender Effekte in Abhängigkeit von Geschlecht und Gesamtaufnahme an Protein (16,21). Bei Kephart et al (37) stellte sich in Verbindung mit 3 aufeinander folgenden intensiven Trainingseinheiten keine Verbesserung regenerativer Marker durch eine Verabreichung von 6g BCAA und 2g Kohlenhydrate heraus, die nicht auch mit der Aufnahme von 42g Kohlenhydraten aus Powerade messbar waren.
Abschließend ein beinahe schon belustigender Auszug einer Gen-Analyse die ich unlängst bei einem Anbieter habe für mich anfertigen lassen. Auch sie spricht sich für den Einsatz von BCAA für eine bessere Regeneration aus. Tolle Sache, wer sich die Empfehlung jedoch genauer ansieht findet die leichte Ungereimtheit hinter der Dosierung. Jeweils 200 Kalorien aus BCAA direkt vor und nach einer Stunde Training (intra)!! Bei einem angenommenen Brennwert von 4,1kcal wie er für Protein verwendet wird ist hier die Rede von knapp 100g BCAA!
Fazit
Lockwood möchte das als „ruiniert“ angesehene Image von BCAA wieder ein wenig zu Recht rücken. Verglichen mit dem Einsatz von EAA oder hochwertigem Protein für den Proteinstoffwechsel gelingt ihm dies leider nicht. Der Einsatz von BCAA für vegane und eiweißarme Ernährung stellt sich verglichen mit dem Einsatz von EAA als weit weniger effektiv heraus. Auch für weitere genannte Einsatzmöglichkeiten wie eine verbesserte Regeneration zeigt sich bestenfalls ein löchriges Bild welches sich weitestgehend auf Versuchen mit Placebos begründet. Inwieweit BCAA pro-regenerativ mehr Effekte versprechen als EAA gilt als nicht hinreichend belegt!
Resümee
Bisher konnte ich nach bestem Wissen und Gewissen noch keine klare Einsatzmöglichkeit von BCAA herausarbeiten, wohl aber Vorteile für die Verwendung von EAA oder vollständigen hochwertigen Proteinquellen, angepasst an den individuellen Tagesbedarf. Sehen wir ob sich dies in Teil 2 noch ändert!
Sportlicher Gruß
Holger Gugg

Quellen
(1)
https://www.peak.ag/de/classic/peak-blog/hbn-eaa-code-warum-wofuer-und-wie
(2)
https://www.ncbi.nlm.nih.gov/pubmed/15930468
(3)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5534203/
(4)
https://academic.oup.com/jn/article/145/9/1981/4585688
(5)
https://www.physiology.org/doi/abs/10.1152/ajpcell.00374.2015
(6)
https://www.frontiersin.org/articles/10.3389/fphys.2017.00390/full
(7)
https://europepmc.org/abstract/med/25617538
(8)
http://www.mdpi.com/2072-6643/9/10/1047/htm
(9)
https://www.ncbi.nlm.nih.gov/pubmed/9124069
(10)
https://www.ncbi.nlm.nih.gov/pubmed/18704484
(11)
https://www.ncbi.nlm.nih.gov/pubmed/7473239
(12)
https://www.ncbi.nlm.nih.gov/pubmed/27468258
(13)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4595234/
(14)
https://www.ncbi.nlm.nih.gov/pubmed/1748109
(15)
https://www.ncbi.nlm.nih.gov/pubmed/11125767
(16)
https://www.ncbi.nlm.nih.gov/pubmed/24967261
(17)
https://www.ncbi.nlm.nih.gov/pubmed/20601741
(18)
https://www.ncbi.nlm.nih.gov/pubmed/22569039
(19)
https://www.ncbi.nlm.nih.gov/pubmed/26853239
(20)
https://www.ncbi.nlm.nih.gov/pubmed/20601741
(21)
http://digitalrepository.unm.edu/educ_hess_etds/66/
(22)
https://www.ncbi.nlm.nih.gov/pubmed/28870476
(23)
https://www.ncbi.nlm.nih.gov/pubmed/15539275
(24)
https://www.ncbi.nlm.nih.gov/pubmed/10198297
(25)
https://www.ncbi.nlm.nih.gov/pubmed/12885705
(26)
https://www.ncbi.nlm.nih.gov/pubmed/9688876
(27)
https://www.ncbi.nlm.nih.gov/pubmed/27208923
(28)
https://www.ncbi.nlm.nih.gov/pubmed/17697406
(29)
https://www.ncbi.nlm.nih.gov/pubmed/2174312
(30)
https://www.ncbi.nlm.nih.gov/pubmed/7723664
(31)
https://www.ncbi.nlm.nih.gov/pubmed/28638350
(32)
https://www.ncbi.nlm.nih.gov/pubmed/16365096
(33)
https://www.ncbi.nlm.nih.gov/pubmed/25827594
(34)
https://www.ncbi.nlm.nih.gov/pubmed/28934166
(35)
https://www.ncbi.nlm.nih.gov/pubmed/21084649
(36)
https://academic.oup.com/ajcn/article/99/1/86/4577382
(37)
https://jissn.biomedcentral.com/articles/10.1186/s12970-016-0142-y
(38)
https://www.frontiersin.org/articles/10.3389/fphys.2015.00245/full
(39)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5096790/
(40)
https://www.ncbi.nlm.nih.gov/pubmed/14651987
(41)
https://www.ncbi.nlm.nih.gov/pubmed/15544573
(42)
https://www.ncbi.nlm.nih.gov/pubmed/16140883
(43)
https://www.sciencedirect.com/science/article/pii/0022480482901263
(44)
https://www.ncbi.nlm.nih.gov/pubmed/19356713
(45)
https://www.ncbi.nlm.nih.gov/pubmed/22560213
(46)
https://www.ncbi.nlm.nih.gov/pubmed/22520843
(47)
http://digitalcommons.wku.edu/ijesab/vol2/iss8/93/
(48)
https://www.body-coaches.de/warum-man-es-mit-bcaa-und-whey-nicht-uebertreiben-sollte
(49)
https://www.ncbi.nlm.nih.gov/pubmed/28145418
(50)
https://www.ncbi.nlm.nih.gov/pubmed/29266268
(51)
https://www.ncbi.nlm.nih.gov/pubmed/27346343
(52)
https://www.ncbi.nlm.nih.gov/pubmed/21169225
(53)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4663614/
(54)
https://www.ncbi.nlm.nih.gov/pubmed/9059905
(55)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3313152/
(56)
https://jissn.biomedcentral.com/articles/10.1186/1550-2783-10-S1-P25
(57)
https://www.ncbi.nlm.nih.gov/pubmed/27346343
(58)
https://www.ncbi.nlm.nih.gov/pubmed/29266268
(59)
https://academic.oup.com/jn/article/141/8/1489/4630526
(60)
https://www.ncbi.nlm.nih.gov/pubmed/7990700
(61)
https://www.ncbi.nlm.nih.gov/pubmed/23097268
(62)
https://academic.oup.com/ajcn/article/87/1/23/4633298
(63)
https://www.ncbi.nlm.nih.gov/pubmed/23587198
(64)
https://www.ncbi.nlm.nih.gov/pubmed/27765690
(65)
L-Isoleucine and L-leucine, may increase glucose uptake through insulin independent effects in healthy, inactive adults
(66)
https://www.ncbi.nlm.nih.gov/pubmed/28444456/
(67)
https://www.ncbi.nlm.nih.gov/pubmed/15596483/
(68)
https://www.ncbi.nlm.nih.gov/pubmed/16424144
(69)
https://www.ncbi.nlm.nih.gov/pubmed/12036812
(70)
https://www.ncbi.nlm.nih.gov/pubmed/11440914
(71)
http://www.mdpi.com/2075-4663/5/2/36
(72)
https://www.ncbi.nlm.nih.gov/pubmed/21512300
(73)
https://www.body-coaches.de/bcaa-vs-proteineaa-es-gibt-nur-einen-sieger
(74)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4700774/
(75)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4865017/
(76)